剑桥研究学者为基因突变过程“建模”,或将推翻达尔文的随机突变理论
科学家对生物基因的突变原因的探索,将会推动未来癌症治疗领域的进步。
近日,剑桥巴布拉罕研究所分子生物学和遗传学专家Jonathan Houseley领导的一个研究小组提出,在酵母研究上,研究人员可以控制酵母基因组的基因突变,尤其是对基因组中具有很强适应能力的基因的控制。
背景
在遗传学研究领域,进化生物学家对突变的解释各执一词,有人表示,突变只是生物在进化过程中自我修复后遗留的些微次要结果;而另有一些研究人员表示,突变率本身的增加是一种演变的结果,有助于生物在压力环境下更快地形成有利于生存的特性。
在众多实验室的研究中,出于由简至繁的研究思路考虑,研究人员采取的研究对象都为单细胞生物。
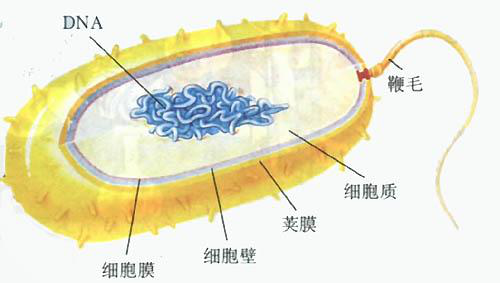
说到生物学上的突变,不得不提到1944年的一件小事,当时哥伦比亚大学遗传学博士生Evelyn M. Witkin偶然间犯了一个错误,她在纽约冷泉港实验室的第一次实验中,不小心将紫外线光调至过亮,以导致数百万的大肠杆菌死亡。但当她检查培养基时,其中有一个培养基,里面有四个大肠杆菌存活了下来并在继续生长。
接下来的二十年间,Witkin一直在研究这些突变体什么时候出现以及为什么出现,因此Witkin在SOS反应的相关研究上获得了一定的成就,但她尚未解决最初提出的问题。
其中,SOS反应,又称应激反应,由克罗地亚人 Miroslav Radman 在1975年发现和命名,是指染色体DNA受到严重损伤时细胞做出的应激反应。
当DNA分子严重损伤时,正常的复制和修复系统无法完成DNA的复制,此时会启动应急反应。在这种情况下,多种基因被诱导表达,其中1个拷贝的UmuC和2个拷贝的被截短的UmuD主要组成 DNA聚合酶Ⅴ,后者可在DNA模板有切口的区域催化DNA复制。
SOS反应包括诱导DNA损伤修复、诱变效应(在DNA受到损伤或复制系统受到抑制的紧急情况下,生物发生突变将有利于其生存)等。该现象广泛存在于原核和真核生物中,主要包括DNA的修复和产生变异。
一直以来,科学家们努力探寻,但始终无法得出生物出现突变的原因,更不敢妄想对基因的突变过程进行控制。
突破
此次,不同于其他人提出的“突变是随机的”等宏大的研究观点,Houseley选择采用定性加定量的方式,对特定种类的突变体进行研究和控制。
2015年,在酵母细胞的研究上,Houseley及其研究团队发现,酵母细胞正在驱动核糖体的部分基因拷贝数的变异。虽然研究团队表示尚无法证明这种变异是细胞对环境变化的有针对性的适应性反应,然而他们发现,当环境中的营养物质丰富时,且蛋白质需求更高时,酵母细胞会催生更多的核糖体基因拷贝。
因此,Houseley制造了相似的环境机制,以检测该环境是否会让酵母细胞有类似的行为。

Houseley
实验中,研究团队专注研究基因CUP1,该基因可以帮助酵母细胞抵制环境中铜的毒性对其的伤害。结果发现,随着环境中铜的增加,细胞中的CUP1基因的拷贝数会增加。但总体来看,大多数细胞的基因拷贝数的增加量没有太大变化,有明显变化的酵母细胞数约占总数的10%。
但研究团队表示,这个实验也许只是巧合,并不能证明一定是环境中的铜引起该基因的突变。
为了让环境中特定因素可以引发突变这一猜想成为必要条件,研究人员巧妙得设计了一种新型的CUP1,使其只受半乳糖影响。实验结果表明,该新型基因的拷贝数随着环境中半乳糖的量的变化而变化,这一发现也并非巧合。
推进
目前,在已有的基因工程研究中,突变过程的机理一致被认为是:当细胞在进行DNA复制时,突变基因的拷贝会停止。而通常停止后会重新开始,即便不能重新开始,该拷贝过程也会接着已有的部分继续拷贝,但在这种情况下,细胞有时会意外删除基因序列或者拷贝过多。
故而,现有的实验室研究团队一致认为是基因组中基因位置的变化直接导致了细胞的重大变异。
但是,Houseley和他的团队认为,虽然这些因素的组合影响使得大家认为拷贝过程中的错误是影响到基因变异的主要因素,但其实这一现象实质上更有可能是在说明,拷贝数是影响突变的主要因素。
不过对于这一猜想,研究团队尚在研究证明中。
Houseley表示,我们的研究就是基于达尔文提出的随机突变,找到影响突变的确切因素,定量分析和引导基因的突变。
总结
对于Houseley的工作,宾夕法尼亚大学的生物学家Paul Sniegowski评价道:“他的工作与该领域的适应性突变争议相关,试着定量分析来证明突变这一不确定现象的确定控制因素是非常棒的想法。但是要想挑战传统的进化理论,他们还需做大量的测试,通过创建一个理论模型来表明突变的演化过程。”
对此,Houseley表示,正在努力,研究阶段尚处于早期阶段。
虽然尚处于尝试证明阶段,但Houseley的想法十分大胆,若研究成功,未来将会改写现有的进化理论,也为未来基因研究、医学治疗等方面,尤其是癌症的控制治疗,带来无法想象的颠覆。
最后,记得关注微信公众号:镁客网(im2maker),更多干货在等你!
硬科技产业媒体
关注技术驱动创新
 基因工程
未来医疗
基因工程
未来医疗

 微信ID:im2maker
微信ID:im2maker
 长按识别二维码关注
长按识别二维码关注